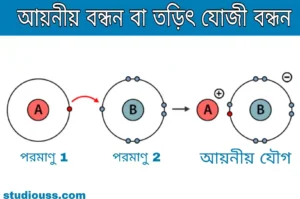
তড়িৎযোজী যৌগ ( lonic compound ) : রাসায়নিক বিক্রিয়ার সময় একাধিক মৌলের পরমাণু ইলেকট্রন গ্রহণ ও বর্জনের মাধ্যমে বিপরীত তড়িৎধর্মী আয়নে পরিণত হয়ে স্থির তড়িদাকর্ষণ বল দ্বারা পরস্পরের সঙ্গে যুক্ত হয়ে যে যৌগ গঠন করে তাকে তড়িৎযোজী যৌগ বলে।
ধাতু ও অধাতুর পরমাণু যুক্ত হয়ে তড়িৎযোজী যৌগ গঠিত হয়। যেমন—সোডিয়াম ক্লোরাইড ( NaCl ), ক্যালশিয়াম অক্সাইড (CaO), ম্যাগনেশিয়াম ক্লোরাইড (MgCl2), পটাশিয়াম সালফাইড (K2S), অ্যালুমিনিয়াম অক্সাইড (Al2O3) ইত্যাদি।
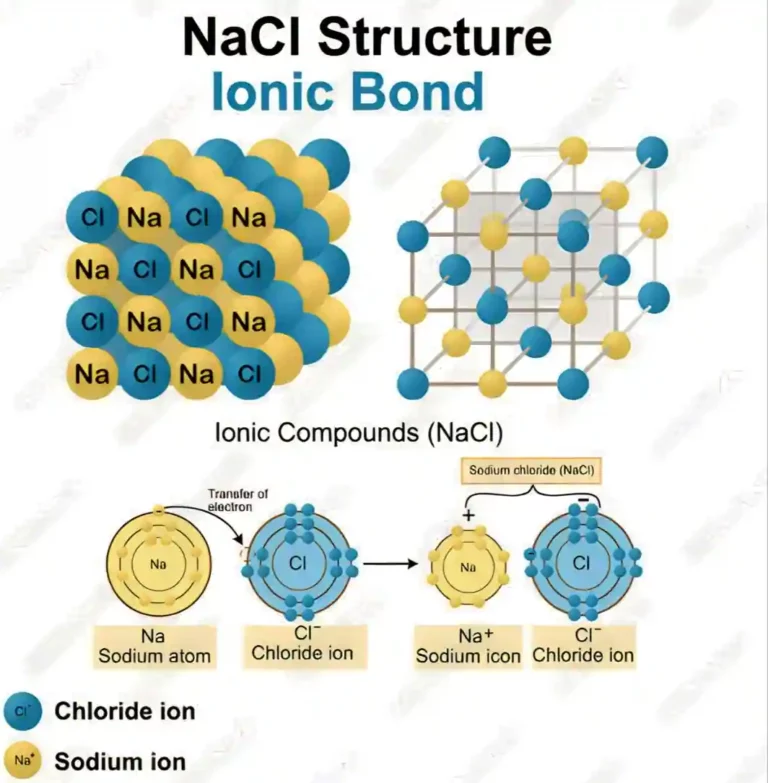
সোডিয়াম ক্লোরাইডের ত্রিমাত্রিক কেলাস গঠন :
সোডিয়াম ক্লোরাইডের কেলাসের মধ্যে এক একটি Na+ আয়নকে 6 টি CI- আয়ন সমান দূরত্বে থেকে সমভাবে ঘিরে থাকে। আবার প্রতিটি Cl- আয়ন সমান দূরত্বে থাকা সমভাবে 6 টি Na + আয়ন দ্বারা পরিবেষ্টিত থাকে, যার ফলে মোট তড়িৎ চার্জ শূন্য হয়।
সোডিয়াম ক্লোরাইডের কেলাস অসংখ্য Na+ এবং CI- আয়ন দ্বারা গঠিত সোডিয়াম ক্লোরাইডের কেলাসে একটি মাত্র সোডিয়াম ক্লোরাইডের অণুর কোনো অস্তিত্ব নেই। আয়নীয় যৌগের কেলাসের দুই প্রান্তে তড়িৎ বিভবপ্রভেদ প্রয়োগ করলেও বিপরীতধর্মী আয়নগুলি তীব্র তাড়িতিক আকর্ষণ বল দ্বারা দৃঢ়ভাবে আবদ্ধ থাকায় আয়নদের যথেষ্ট আপেক্ষিক সরণ ঘটে না। এই কারণেই গলিত বা দ্রবীভূত অবস্থার তুলনায় কঠিন অবস্থায় আয়নীয় যৌগের তড়িৎ পরিবাহিতা খুব কম হয়।
Note:- প্রতিটি আয়নীয় যৌগের কেলাস অসংখ্য ক্যাটায়ন ও অ্যানায়ন দ্বারা গঠিত একটি সুস্থিত ত্রিমাত্রিক আকারবিশিষ্ট হওয়ায় আয়নীয় যৌগে কোনো অণুর অস্তিত্ব থাকে না। তাই আয়নীয় যৌগের ক্ষেত্রে আণবিক ভরের পরিবর্তে সংকেত ভর কথাটি প্রযোজ্য। তাই সোডিয়াম ক্লোরাইডের আণবিক ভর 58.5 না বলে সংকেত ভর 58.5 বলা হয়।
Covered Topics:- সোডিয়াম ক্লোরাইড এর কেলাস গঠন, NaCl এর গঠন ব্যাখ্যা, সোডিয়াম ক্লোরাইডের ত্রিমাত্রিক গঠন বর্ননা কর, সোডিয়াম ক্লোরাইড এর কেলাস গঠন, সোডিয়াম ও ক্লোরিনের যৌগ গঠন, Nacl এর গঠন ব্যাখ্যা কর, Nacl এর কেলাস গঠন চিত্র, NaCl এর গলনাংক ও স্ফুটনাংক।



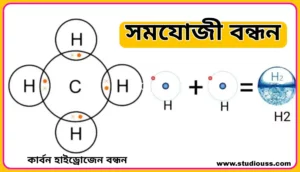
Pingback: সমযোজী বন্ধন কাকে বলে | সমযোজী বন্ধন কয় প্রকার ও কি কি | সমযোজী বন্ধনের বৈশিষ্ট্য – Studious
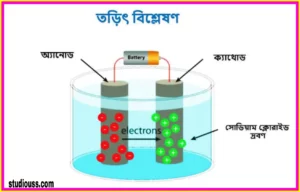
Pingback: তড়িৎ বিশ্লেষণ (Electrolysis) কাকে বলে | জলের তড়িৎ বিশ্লেষণ বর্ণনা কর – Studious