হ্যালো বন্ধুরা, আজ আমরা আলোচনা করবো রাদারফোর্ডের আলফা কণা বিচ্ছুরণ পরীক্ষা সমন্ধে। রাদারফোর্ডের আলফা কণা বিচ্ছুরণ পরীক্ষার পর্যবেক্ষণ ও সিদ্ধান্ত আরও জানবো রাদারফোর্ডের পরীক্ষা থেকে কীভাবে তিনি এই সিদ্ধান্তে উপনীত হন যে পরমাণুর অধিকাংশ স্থানই ফাঁকা।
রাদারফোর্ডের পরীক্ষা (Rutherford’s α- particle experiment)
রাদারফোর্ডের আলফা কণা বিচ্ছুরণ পরীক্ষা থেকে পরমাণুর গঠন সম্বন্ধে ধারণা পাওয়া যায়। রাদারফোর্ডের আলফা কণা বিক্ষেপণ পরীক্ষা সম্বন্ধে বিস্তারিত তথ্য জানার আগে তেজস্ক্রিয়তা সম্বন্ধে কিছু ধারণা লাভ করা দরকার
তেজস্ক্রিয়তার আবিষ্কার (Discovery of radioactivity)
বিজ্ঞানী হেনরী বেকারেল ( Henry Becquerel ) ইউরেনিয়াম ঘটিত একটি লবণকে (পটাশিয়াম ইউরানিল সালফেট) একটি মােটা কালাে কাগজে মুড়ে একটি ফোটোগ্রাফিক প্লেটের উপর রেখে দেন। কয়েকদিন পরে তিনি দেখেন যে ফোটোগ্রাফিক প্লেটে ওই লবণের একটি ছবি উঠেছে।
তিনি ভাবতে থাকেন এটি কীভাবে সম্ভব হল ? পরে তিনি একটি সিদ্ধান্তে আসেন যে, ওই লবণ থেকে একটি অদৃশ্য রশ্মি স্বতঃস্ফূর্তভাবে সবসময় নির্গত হয় যা ফোটোগ্রাফিক প্লেটকে আক্রান্ত করে। এই রশ্মির নাম দেওয়া হয় তেজস্ক্রিয় রশ্মি ( Radioactive ray )। ইউরেনিয়াম, রেডিয়াম, থােরিয়াম প্রভৃতি উচ্চ আণবিক ভরবিশিষ্ট মৌলগুলি থেকে এই তেজস্ক্রিয় রশ্মি নির্গত হয়। এই মৌলগুলিকে বলে তেজস্ক্রিয় মৌল (Radioactive element)। মৌলগুলির তেজস্ক্রিয় রশ্মি নির্গমনের ধর্মকে বলে তেজস্ক্রিয়তা ( Radioactivity )।
তেজস্ক্রিয় রশ্মি তিন প্রকারের হয়, যেমন — আলফা রশ্মি , বিটা রশ্মি এবং গামা রশ্মি। আলফা রশ্মি হল ধনাত্মক আধানযুক্ত হিলিয়াম কণার স্রোত। প্রতিটি আলফা কণার ভর 4 একক এবং চার্জ + 2 একক।
রাদারফোর্ডের পরীক্ষা ( Rutherford’s experiment ) :
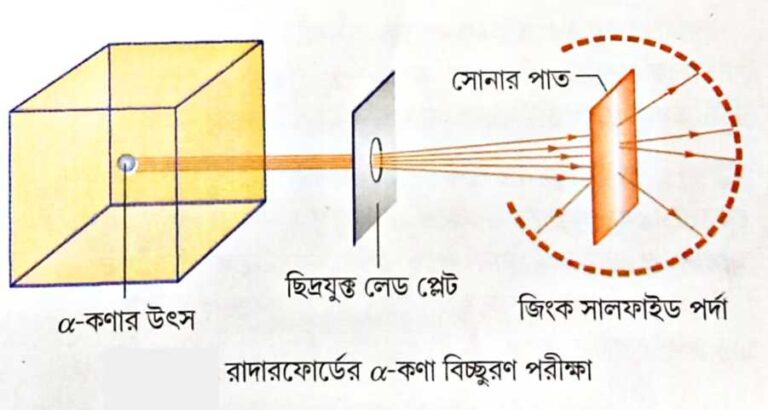
বিজ্ঞানী রাদারফোর্ড 0.0004 মিমি ( খুব পাতলা ) বেধবিশিষ্ট সােনার পাতের ওপর তেজস্ক্রিয় আইসােটোপ ( 83Bi214 ) থেকে নির্গত উচ্চ গতিসম্পন্ন আলফা রশ্মি চালনা করেন। পাতটির পেছনে একটি জিংক সালফাইডের প্রলেপ দেওয়া পর্দা রাখা হয়। আলফা রশ্মি এই পর্দার ওপর পড়লে উজ্জ্বল আলােকবিন্দু সৃষ্টি করে। পরীক্ষাটি একটি আবদ্ধ বায়ুশূন্য পাত্রে ঘটানাে হয়।
রাদারফোর্ড পরীক্ষার পর্যবেক্ষণ (Observation) :
রাদারফোর্ড লক্ষ করেন—
1 ) বেশিরভাগ আলফা কণা ( প্রায় 99 % ) সােনার পাত ভেদ করে সােজা বেরিয়ে পর্দার ওপরে পড়ে কিন্তু পাতের গায়ে কোনাে ছিদ্র হয় না।
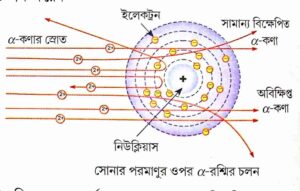
2 ) কিছু আলফা কণা সামান্য কোণে বিক্ষিপ্ত হয়ে ডানদিকে বা বামদিকে বেঁকে যায়।
3 ) অল্প সংখ্যক আলফা কণা 90 ° বা তার বেশি কোণে বিক্ষিপ্ত হয়।
4 ) দু – একটি আলফা- কণা ( প্রায় 20,000 – এর মধ্যে একটি ) যে পথে যায় সেই পথে আবার ফিরে আসে অর্থাৎ এক্ষেত্রে আলফা বিচ্যুতি 180 ° হয়।
রাদারফোর্ড পরীক্ষার সিদ্ধান্ত
উপরােক্ত পরীক্ষা থেকে রাদারফোর্ড এই সিদ্ধান্তে আসেন যে—
1) যেহেতু অধিকাংশ আলফা কণা কোনােদিকে বিক্ষিপ্ত না হয়ে সােজাপথে বেরিয়ে আসে অতএব পরমাণু নিরেট নয় , পরমাণুর বেশিরভাগ স্থানই ফাঁকা।
2 ) যে আলফা কনাগুলি সামান্য কোণে বিক্ষিপ্ত হয় সেগুলি পরমাণুর ভিতর কোনাে ধনাত্মক আধানের কাছ দিয়ে যায় , এর ফলে আলফা কণার সামান্য বিক্ষেপণ ঘটে।
3 ) ধনাত্মক আধান ধনাত্মক আধানকে বিকর্ষণ করে। আলফা রশ্মি ধনাত্মক আধানযুক্ত কণা। সুতরাং, গতিশীল ভারী আধানযুক্ত আলফা কণাকে তার গতির বিপরীতে ফিরিয়ে দিতে পারে অপর এক ভারী ধনাত্মক আধাগ্রস্ত কণা।
আবার মাত্র 20,000 – এর মধ্যে যেহেতু একটি আলফ কণা যে পথে যায় সেই পথেই ফিরে আসে সেহেতু প্রমাণিত হয় যে, পরমাণুর সমগ্র আয়তনের তুলনায় অতি ক্ষুদ্র এক স্থানে পরমাণুর ধনাত্মক আধান ( প্রােটন ) ও পরমাণুর প্রায় সমগ্র ভর কেন্দ্রীভূত আছে। একে নিউক্লিয়াস বা পরমাণুকেন্দ্রক বলে।
4 ) ইলেকট্রনগুলি নিউক্লিয়াসের বাইরে ফাঁকা স্থানে অবস্থান করে। অধিকাংশ আলফা কণা যখন ওই ফাকা স্থানের মধ্য দিয়ে যায় তখন ইলেকট্রন দ্বারা আলফা কণা আকৃষ্ট হয়। কিন্তু আলফা কণার ভর ইলেকট্রনের তুলনায় অনেক বেশি বলে ইলেকট্রনের আকর্ষণ আলফা গতিপথকে প্রভাবিত করতে পারে না। এজন্য অধিকাংশ আলফা কণা সােজা পথে বেরিয়ে আসে।



Good
Thank you
good
বই এ খুঁজে পাচ্ছিলাম না। ধন্যবাদ
Pingback: ক্যালোরিমিতির মূলনীতি (Principles of Calorimetry) | ক্যালোরিমিটার কি? – Studious
Pingback: নিউক্লিয় বল (Nuclear Force) কাকে বলে? | বৈশিষ্ট্য ও প্রকৃতি – Studious
many many thanks
we are always here to give our visitors a quality and informative content
Thank you very much
visit again